Klinische Studien sind Der Eckpfeiler der modernen medizinischen Forschung dient als Beweismittel für den Nachweis (oder die Widerlegung) der Sicherheit und Wirksamkeit einer neuen Behandlung. Klinische Studien sind jedoch auch kostspielige und ressourcenintensive Unternehmungen, bei denen es viele Jahre dauern kann, bis ein Medikament oder Gerät als bereit für die breite Markteinführung gilt.
Das ist etwas, das Lindus Gesundheit macht sich an die Arbeit und präsentiert sich selbst als „Auftragsforschungsorganisation der nächsten Generation“ (CRO), die die Durchführung klinischer Studien schneller und einfacher macht. Das britische Startup gab heute bekannt, dass es in einer Serie-A-Finanzierungsrunde 18 Millionen US-Dollar von namhaften Geldgebern wie dem Spotify-Investor Creandum und dem milliardenschweren Unternehmer Peter Thiel eingesammelt hat.
Lindus wurde 2021 in London gegründet und entstand aus Beobachtungen und Frustrationen, die zwei der Firmengründer direkt erlebten. Ein ehemaliger Risikokapitalgeber bei Omers Ventures, Meri Beckwith Durch seine Arbeit mit Startups im Bereich Gesundheitstechnologie hatte er direkte Kenntnisse über klinische Studien.
„Ich habe eine Zeit lang im Risikokapitalbereich gearbeitet und bin dabei auf Unternehmen gestoßen, die ihre eigenen klinischen Studien durchführen“, erklärte Beckwith gegenüber Tech. „Alle waren allgemein mit den Ergebnissen frustriert. Alle beschwerten sich ständig darüber, wie lange klinische Studien dauerten, dass die Ergebnisse immer schlecht waren und dass es immer Fehler gab. Als Investor hielt ich dies für einen wirklich interessanten Investitionsbereich.“
Als sich im Jahr 2020 die globale Pandemie ausbreitete, meldete sich Beckwith auch freiwillig zur Teilnahme an mehreren COVID-Impfstoffstudien und erhielt so Einblicke aus erster Hand in den Prozess klinischer Studien.
„Ich war völlig schockiert, als ich sah, wie unglaublich dysfunktional das war“, fügte Beckwith hinzu. „Und das war eines der wirklich großen, gut finanzierten Projekte Phase drei Versuche. Ich erinnere mich, dass ich den Internet Explorer herunterladen musste, um mich überhaupt für die klinische Studie anzumelden. Die vom CRO erstellte Website basierte auf WordPress und verfügte über kein SSL-Zertifikat. Und was die klinischen Studien angeht, waren es nur haufenweise lächerliche Fehler. Das war wirklich ein Augenöffner.“
Michael Young, einer der beiden anderen Gründer von Lindus, war früher als Sonderberater in Downing Street tätig und unterstützte den Premierminister und die britische Regierung in unzähligen Fragen im Bereich der Biowissenschaften. Während er viel an der Arbeit rund um Gesundheit und Biotechnologie beteiligt war, sagte Young, dass sich ein Großteil der Überlegungen auf Arzneimittelzulassungen und die Einführung des NHS konzentrierte und nicht auf „das gewisse Etwas dazwischen“ – also darauf, wie die klinischen Studien tatsächlich durchgeführt werden .
„Darüber haben wir einfach überhaupt nicht nachgedacht“, sagte Young gegenüber Tech. „Und es war diese Erfahrung, die mich dazu brachte, mich intensiver damit zu befassen, was bei klinischen Studien tatsächlich passiert. Wir kamen zu dem Schluss, dass DAS der Engpass ist, der verhindert, dass all die wirklich coolen F&E-Sachen, die passieren, zu den Patienten gelangen.“
Klinische Anzeichen
Es gibt zahlreiche Neugründungen, die sich im Bereich der technologieorientierten klinischen Studien einen Namen machen wollen, darunter risikokapitalfinanzierte Unternehmen wie Science 37, Koneksa, Curebase und Florence Healthcare, um nur einige zu nennen. Das Hauptverkaufsargument von Lindus Health besteht jedoch darin, dass das Unternehmen den gesamten End-to-End-Prozess bei der Durchführung klinischer Studien abdecken will und nicht auf spezifische „Punktlösungen“ setzt.
„Die Unternehmen, mit denen wir konkurrieren, sind die großen CROs“, sagte Young. „Dies ist ein riesiger Markt, und technologieorientierte CROs haben noch nicht Fuß gefasst.“
Zum Vergleich: Eine Auftragsforschungsorganisation (Contract Research Organization, CRO) ist ein Drittunternehmen, an das Pharma-, Biotech- und Medizingeräteunternehmen einen Teil ihrer geschäftskritischen Arbeit auslagern, beispielsweise die klinische Forschung. Dies erspart ihnen die Notwendigkeit, die gesamte Arbeit intern selbst zu erledigen, und kann sich ausschließlich auf ihre Kernproduktentwicklung konzentrieren. Der CRO-Markt ist bedeutend, wird heute als 77-Milliarden-Dollar-Markt eingestuft mit Prognosen, dass es innerhalb von fünf Jahren um 70 % wachsen wird. Bemerkenswerte Spieler sind: IQVIAdas sich zu einem 40-Milliarden-Dollar-Giganten im CRO-Bereich entwickelt hat und seine Marktkapitalisierung in den letzten Jahren verdoppelt hat.
Eine typische klinische Studie umfasst den anfänglichen Versuchsentwurf, einschließlich der Erstellung eines Protokolls und eines Pakets zur behördlichen Einreichung; Aufbau der Technologieplattform zur Durchführung der Versuche; Rekrutierung von Patienten; Bereitstellung des Programms; und das Sammeln aller Daten. Jede Phase kann je nach Größe und Umfang einer klinischen Studie Jahre dauern. Deshalb ist Lindus bestrebt, alles zu rationalisieren – mit Ausnahme des Ethik- und Regulierungsprozesses, der unter der Kontrolle Dritter steht – und das Bestehende zu verbessern Software für klinische Studien auf dem Markt.
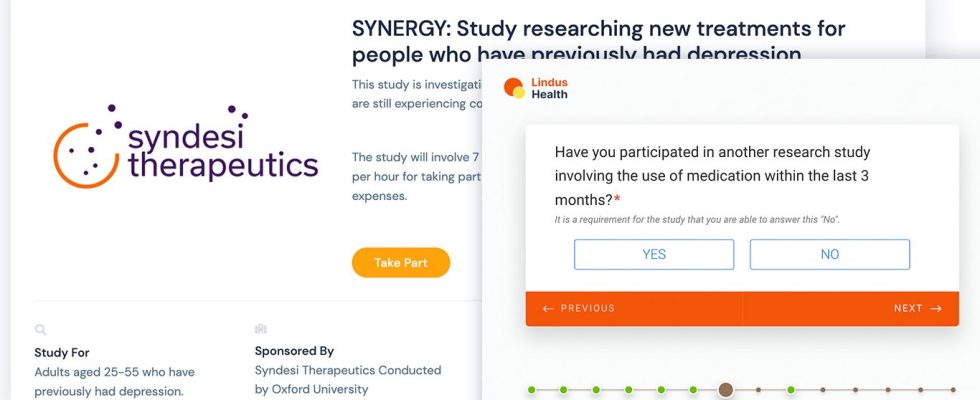
„Es ist ein Klischee, dass Websites (auf denen klinische Studien stattfinden) die Software auf dem Markt hassen“, sagte Young. „Wir haben Tausende von Stunden in Gespräche mit Website-Benutzern investiert, um sicherzustellen, dass unser Tool intuitiv ist und die grundlegenden Aufgaben, die sie ausführen, automatisiert. Dies führt zu engagierteren Websites und damit zu einer schnelleren Rekrutierung und besseren Daten.“
Lindus Health: Rekrutierung Bildnachweise: Lindus Gesundheit
Ein Teil dieses Rationalisierungsprozesses basiert auf maschinellem Lernen (ML), auch in der ersten Phase des Protokollschreibens, die laut Young typischerweise ein sehr „manueller iterativer Prozess“ ist.
„Das Ergebnis ist, dass es trotz der besten Absichten zu Widersprüchen oder sogar scheinbar sinnvollen Ergänzungen kommen kann, die einen Prozess behindern“, sagte er. „Zum Beispiel das Hinzufügen so vieler Ausschlusskriterien, dass es fast unmöglich ist, für eine Studie Rekruten zu gewinnen.“
Daher hat Lindus ein Tool zur „Protokollgenerierung“ entwickelt, das sich derzeit im Proof-of-Concept-Stadium befindet und zusätzlich zu den daraus gewonnenen Protokollen auf seinen eigenen historischen Protokollen trainiert Clinicaltrials.gov, um laut Young einen „ersten Protokollentwurf basierend auf einer kleinen Anzahl von Eingaben“ zu erstellen. „Wir können dies dann durch ein separates Modell laufen lassen, das wir anhand öffentlicher Daten trainiert haben ScanMedicine das die Studienrisiken hervorhebt und Vorschläge zur Verbesserung der Studie macht.“
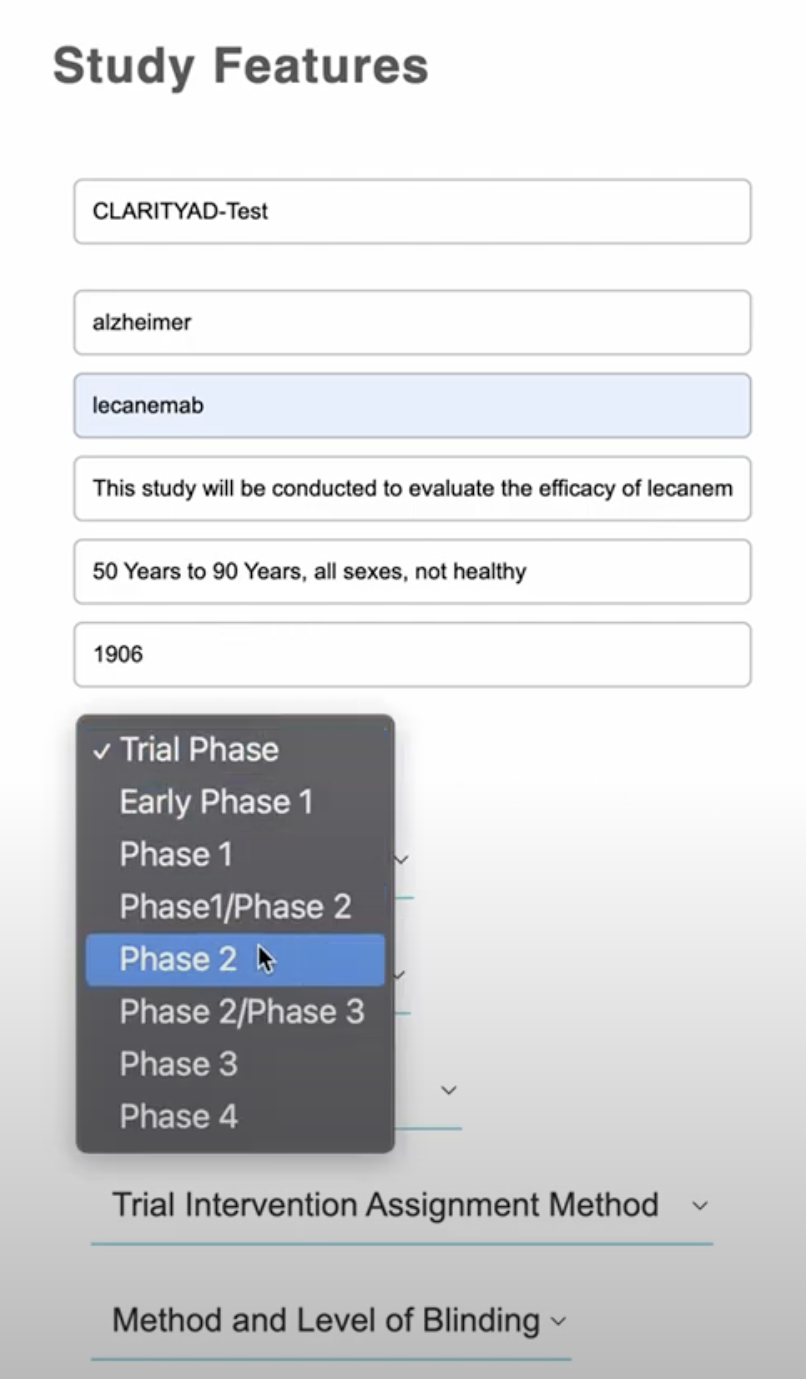
Lindus Health AI-Protokolltool Bildnachweise: Lindus Gesundheit
Die Datenerfassung ist ein wichtiger Teil des Prozesses klinischer Studien. Lindus unterstützt dies, indem es dem Studienpersonal ermöglicht, alle Daten von Anfang an elektronisch zu erfassen, den Prozess mithilfe von KI zu überwachen und zu verwalten und gleichzeitig die Vollständigkeit und Richtigkeit der Daten zu überprüfen. Zu diesem Zweck habe das Unternehmen laut Young eine Reihe von Modellen trainiert, um Daten bei der Aufnahme in Echtzeit zu analysieren.
Lindus stellt alle diese Daten in einem zentralen Dashboard zur Verfügung.
„Klinische Studien sind im Wesentlichen nur eine Datenerfassungsübung“, sagte Young. „Eine standardmäßige klinische Studie wird Hunderttausende bis Millionen Datenpunkte generieren. Das Unternehmen, das eine klinische Studie durchführt, ist dafür verantwortlich, sicherzustellen, dass diese Daten korrekt sind und dass alle Daten identifiziert werden, die auf ein Risiko für die Patientensicherheit hinweisen könnten.“
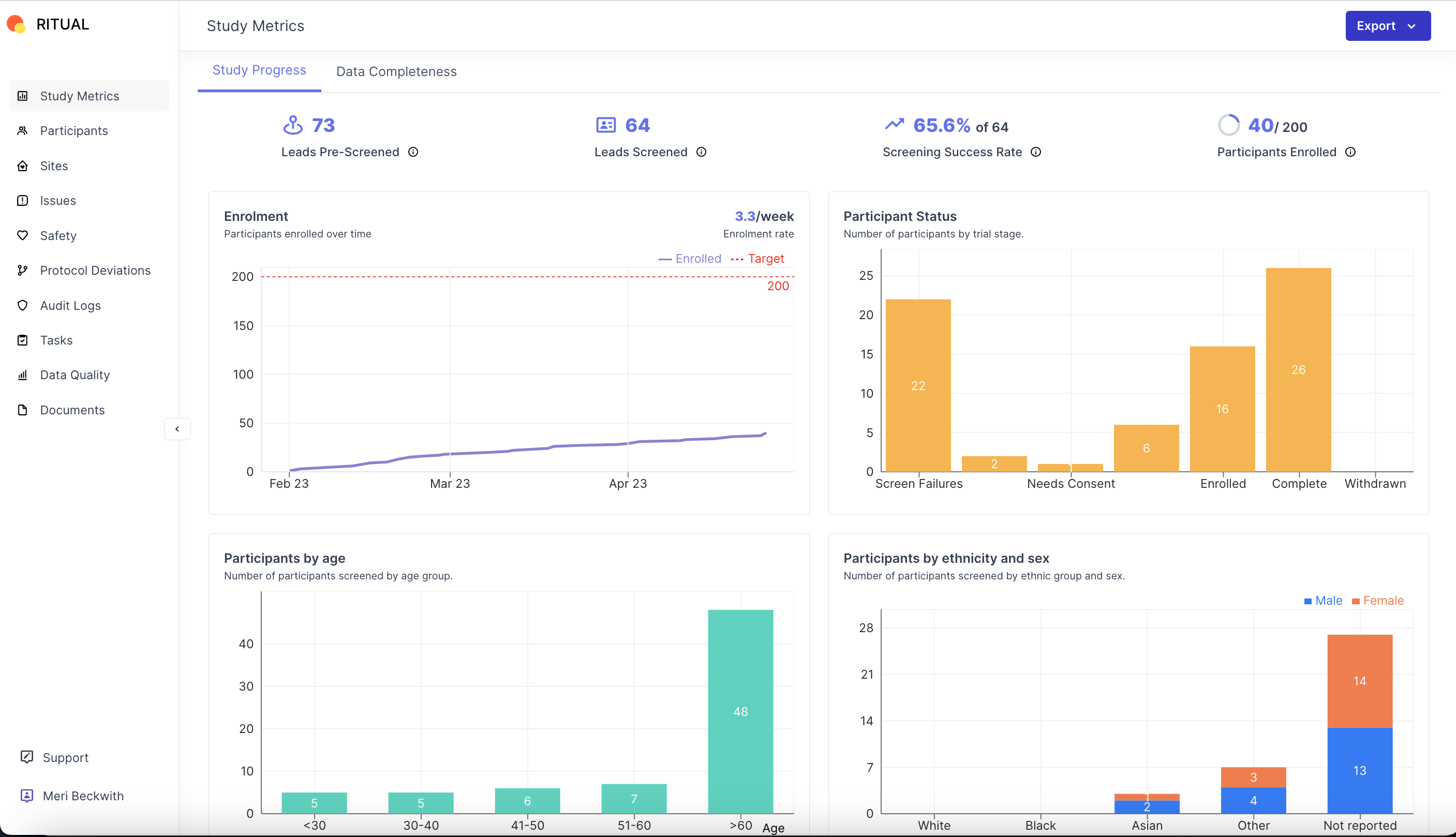
Lindus Health-Studiendaten-Dashboard Bildnachweise: Lindus Gesundheit
Menschlicher Zustand
Lindus hatte bisher rund 6 Millionen US-Dollar an Finanzmitteln von denselben Investoren eingesammelt, die sich auch der Serie-A-Runde angeschlossen hatten, darunter Creandum und Peter Thiel. Mit weiteren 18 Millionen US-Dollar auf der Bank ist das Unternehmen nun gut ausgestattet, um seine Präsenz in Europa und Nordamerika auszubauen, wo es nach eigenen Angaben seit seiner Gründung vor zwei Jahren bereits mehr als 80 klinische Studien durchgeführt hat.
Bisher hat sich Lindus auf eine Handvoll Erkrankungen konzentriert, darunter Depressionen, Diabetes und Schlaflosigkeit. Laut Beckwith gibt es verschiedene Faktoren, die bestimmen, welche Bedingungen unterstützt werden, aber es kommt vor allem darauf an, konzentriert zu bleiben und nicht zu versuchen, alles auf einmal zu erledigen.
„Auf der praktischen Seite ist unser Northstar – und was uns von vielen anderen Unternehmen in diesem Bereich unterscheidet –, dass wir immer fest daran geglaubt haben, dass wir die gesamte klinische Studie durchführen müssen, um etwas zu bewirken und etwas zu bewirken CROs verdrängen“, sagte Beckwith. „Dann dachten wir als Startup: ‚Was sind die einfachsten klinischen Studien, die wir durchführen können, bei denen wir trotzdem die Leitung der gesamten klinischen Studie übernehmen können?‘“
Daher hat Lindus absichtlich versucht, häufiger auftretende Erkrankungen zu unterstützen. Während sich das Unternehmen zunächst auf nicht-medikamentöse Produkte konzentrierte, die von Natur aus weniger Hürden bei der Durchführung klinischer Studien mit sich bringen, hat es sich inzwischen auf Arzneimittelprodukte ausgeweitet und versucht nun auch, die Unterstützung auf andere Erkrankungen wie Tinnitus, Schlaflosigkeit, Wechseljahre und Kurzsichtigkeit bei Kindern auszudehnen.
Beckwith fügte hinzu, dass die Pharmaindustrie ihre Forschung und Entwicklung in den letzten Jahren auf mehr Nischenerkrankungen und seltene Krankheiten konzentriert habe, was dazu geführt habe, dass häufigere Erkrankungen wie Typ-2-Diabetes vernachlässigt wurden.
„Möglicherweise liegt der Grund dafür in der Infrastruktur für klinische Studien, da die Durchführung klinischer Studien für jeden Patienten mit so hohen Kosten verbunden ist“, sagte Beckwith. „Aus wirtschaftlicher Sicht ist es für sie daher nur sinnvoll, klinische Studien durchzuführen, bei denen man mit wenigen Patienten eine Genehmigung erhalten kann und diese Genehmigung zu einem enormen Dollarwert für eine Behandlungsreihe führt. Daher glauben wir, dass unser größter Wettbewerbsvorteil darin besteht, dass wir klinische Studien insgesamt viel skalierbarer gemacht haben.“
Regulierungszeit
Lindus hat eine Reihe von Unterstützern aus verschiedenen Bereichen des VC-Spektrums gewonnen, darunter die oben genannten Creandum, Firstminute Capital, Seedcamp, Hambro Perks und Amino Collective. Aber Peter Thiel ist angesichts seiner Erfolgsbilanz im Bereich Gesundheitstechnologie wohl der bemerkenswerteste Teilnehmer.
„Wir sind über einen unserer Angel-Investoren mit Peter in Kontakt gekommen, und als wir uns zum ersten Mal unterhalten haben, hat er sich sehr intensiv mit dem Verständnis des Marktes befasst erste Prinzipien“, sagte Beckwith. „Zum Beispiel, warum der Markt so aussieht, wenn die aktuellen CROs ein schreckliches Angebot haben und ein Oligopol haben. Und Peters Due-Diligence-Prüfung, oder „Prozess“, wenn Sie so wollen, unterschied sich stark von der praktisch aller anderen Investoren, mit denen wir gesprochen haben, was ziemlich erfrischend ist. Im Wesentlichen drehten sich alle Fragen um die Frage: „Wie groß könnte Lindus Health sein, wenn es uns gut geht?“
Die Tatsache, dass Thiel wie die meisten Seed-Investoren von Lindus Health seine Investitionen verdoppelt hat, ist ein Hinweis darauf, wie er den Status quo der klinischen Studien beurteilt. In der Tat, wie bei fast jedem selbsternannt Als Libertärer war Thiel nie jemand, der Regulierung mit offenen Armen begrüßte. Er ist aber auch ein großer Befürworter des medizinischen Fortschritts, in den er investiert unzählige Biotech-Unternehmen als Teil eines längerfristigen Plans, um, nun ja, für immer leben. Daher äußerte Thiel lautstark die Hürden, die es mit sich bringt, neue Medikamente auf den Markt zu bringen. Das beinhaltet Lambasting die US-amerikanische Food and Drug Administration (FDA) darüber, wie es behindert verhinderte, dass experimentelle Medikamente auf den Markt kamen, und er sorgte auch für Aufsehen, als er in ein Unternehmen investierte, das seine klinischen Studien zuvor ins Ausland verlagert und sich der Aufsicht der FDA entzogen hatte.
Allerdings gibt es in der Regel aus gutem Grund Regeln und Aufsicht, insbesondere wenn es um Arzneimittelstudien geht. Daher könnte jedes Unternehmen, das verkündet, es würde eine Branche, die für ihre Regulierungsaufsicht bekannt ist, auf den Kopf stellen, mit etwas Misstrauen betrachtet werden. Aber Young besteht darauf, dass sie sich ausschließlich auf die Lösung technischer und prozessbezogener Probleme konzentrieren und nicht versuchen, eine Änderung der Vorschriften voranzutreiben, was seiner Meinung nach für ein Startup „ein aussichtsloser Kampf“ wäre. In Wahrheit ist Lobbyismus dieser Art etwas Die großen Pharmaunternehmen selbst werden dies wahrscheinlich eher verfolgen.
„Die Vorschriften für klinische Studien entwickeln sich zwar weiter, aber nichts von dem, was wir tun, befindet sich in einer Grauzone“, sagte er. „Wir glauben auf jeden Fall, dass die Regulierungsbehörden mehr tun könnten, um Sponsoren zur Innovation zu ermutigen – aber innerhalb eines bestehenden Regulierungsrahmens.“