Google DeepMind hat eine neue Version von AlphaFold vorgestellt, seinem transformativen Modell für maschinelles Lernen, das die Form und das Verhalten von Proteinen vorhersagt. AlphaFold 3 ist nicht nur genauer, sondern sagt auch Wechselwirkungen mit anderen Biomolekülen voraus, was es zu einem weitaus vielseitigeren Forschungsinstrument macht – und das Unternehmen stellt eine eingeschränkte Version des Modells kostenlos zur Online-Nutzung zur Verfügung.
Seit der Einführung des ersten AlphaFold im Jahr 2018 ist das Modell die führende Methode zur Vorhersage der Proteinstruktur anhand der Sequenz der Aminosäuren, aus denen sie bestehen.
Obwohl dies eher eine eng gefasste Aufgabe zu sein scheint, ist es für fast die gesamte Biologie von grundlegender Bedeutung, Proteine – die in unserem Körper eine nahezu endlose Vielfalt an Aufgaben erfüllen – auf molekularer Ebene zu verstehen. In den letzten Jahren haben rechnergestützte Modellierungstechniken wie AlphaFold und RoseTTaFold teure, laborbasierte Methoden abgelöst und die Arbeit Tausender Forscher in ebenso vielen Bereichen beschleunigt.
Aber die Technologie ist noch in vollem Gange, und jedes Modell ist „nur ein Schritt auf dem Weg“, wie DeepMind-Gründer Demis Hassabis es in einer Pressekonferenz zum neuen System ausdrückte. Das Unternehmen hat die Veröffentlichung Ende letzten Jahres angekündigt, aber dies ist sein offizielles Debüt.
Ich überlasse es den Wissenschaftsblogs, genau darauf einzugehen, wie das neue Modell die Ergebnisse verbessert, aber an dieser Stelle genügt es zu sagen, dass AlphaFold 3 durch eine Vielzahl von Verbesserungen und Modellierungstechniken nicht nur genauer, sondern auch umfassender anwendbar ist.
Eine der Einschränkungen der Proteinmodellierung besteht darin, dass selbst wenn man weiß, wie eine Aminosäuresequenz aussehen wird, das nicht unbedingt bedeutet, dass man weiß, an welche anderen Moleküle sie sich bindet und wie. Und wenn man mit diesen Molekülen tatsächlich Dinge tun wollte, was bei den meisten der Fall ist, musste man das durch aufwändigere Modellierung und Tests herausfinden.
„Biologie ist ein dynamisches System, und man muss verstehen, wie Eigenschaften der Biologie dadurch entstanden sind Interaktionen zwischen verschiedenen Molekülen in der Zelle. Und Sie können sich AlphaFold 3 als unseren ersten großen Schritt in diese Richtung vorstellen“, sagte Hassabis. „Es ist in der Lage, Proteine zu modellieren, die natürlich mit anderen Proteinen interagieren, aber auch mit anderen Biomolekülen, darunter vor allem DNA- und RNA-Stränge.“
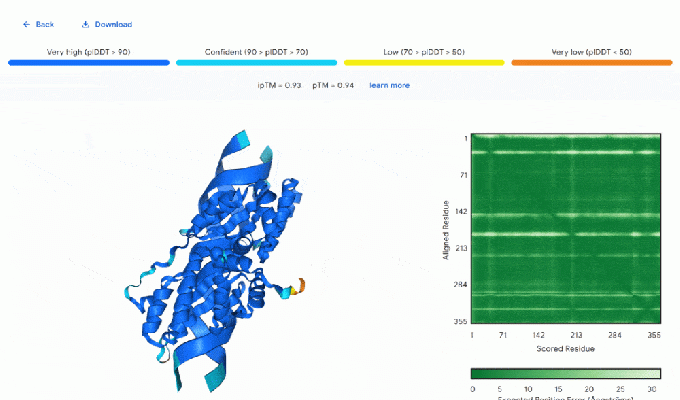
Mit AlphaFold 3 können mehrere Moleküle gleichzeitig simuliert werden – zum Beispiel ein DNA-Strang, einige DNA-bindende Moleküle und vielleicht ein paar Ionen, um die Sache aufzupeppen. Folgendes erhält man für eine solche spezifische Kombination: Die DNA-Bänder verlaufen in der Mitte, die Proteine glänzen an der Seite, und ich denke, das sind die Ionen, die dort in der Mitte wie kleine Eier eingebettet sind:
Dies ist an sich natürlich keine wissenschaftliche Entdeckung. Aber selbst herauszufinden, ob ein experimentelles Protein überhaupt oder auf diese Weise binden oder sich in diese Form verbiegen würde, war im Allgemeinen die Arbeit von mindestens Tagen oder vielleicht Wochen bis Monaten.
Auch wenn die Aufregung in diesem Bereich in den letzten Jahren kaum zu überschätzen ist, waren die Forscher durch den Mangel an Interaktionsmodellierung (von der die neue Version eine Form bietet) und die Schwierigkeiten bei der Implementierung des Modells größtenteils gelähmt.
Dieses zweite Problem ist vielleicht das größere von beiden, denn obwohl die neuen Modellierungstechniken in gewissem Sinne „offen“ waren, sind sie wie andere KI-Modelle nicht unbedingt einfach bereitzustellen und zu bedienen. Aus diesem Grund bietet Google DeepMind AlphaFold Server an, eine kostenlose, vollständig gehostete Webanwendung, die das Modell für die nichtkommerzielle Nutzung verfügbar macht.
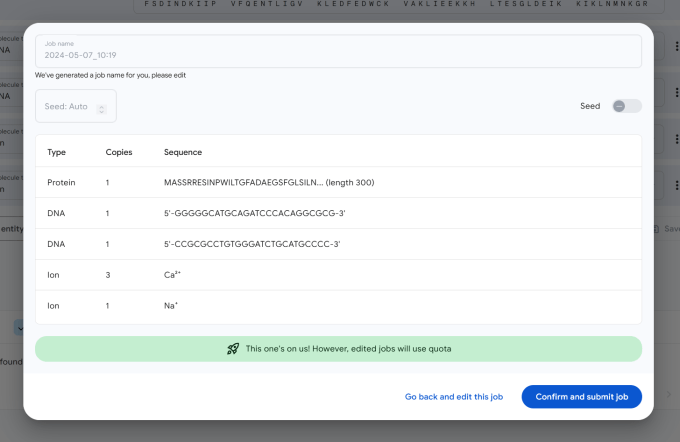
Es ist kostenlos und recht einfach zu verwenden – ich habe es in einem anderen Fenster während des Anrufs gemacht, während sie es erklärt haben (so habe ich das Bild oben erhalten). Sie benötigen lediglich ein Google-Konto und geben dann so viele Sequenzen und Kategorien ein, wie es verarbeiten kann – es gibt einige Beispiele – und senden es ab. In wenigen Minuten sollte Ihre Arbeit erledigt sein und Sie erhalten ein lebendes 3D-Molekül, dessen Farbe das Vertrauen des Modells in die Konformation an dieser Position darstellt. Wie Sie in der Abbildung oben sehen können, sind die Spitzen der Bänder und die Teile, die stärker unerwünschten Atomen ausgesetzt sind, heller oder rot, um weniger Vertrauen anzuzeigen.
Ich fragte, ob es einen wirklichen Unterschied zwischen dem öffentlich zugänglichen Modell und dem intern verwendeten Modell gebe. Hassabis sagte: „Wir haben den Großteil der Fähigkeiten des neuen Modells verfügbar gemacht“, ging aber nicht näher darauf ein.
Es liegt eindeutig daran, dass Google sein Gewicht in die Waagschale wirft – und dabei bis zu einem gewissen Grad die besten Teile für sich behält, was natürlich ihr Vorrecht ist. Um ein kostenloses, gehostetes Tool wie dieses zu erstellen, müssen erhebliche Ressourcen für diese Aufgabe aufgewendet werden – täuschen Sie sich nicht, dies ist eine Geldgrube, eine (für Google) teure Shareware-Version, um die Forscher auf der ganzen Welt davon zu überzeugen, dass AlphaFold 3 überhaupt sein sollte Zumindest einen Pfeil in ihrem Köcher.
Das ist jedoch in Ordnung, denn die Technologie wird wahrscheinlich Geld über die Alphabet-Tochtergesellschaft Isomorphic Labs drucken (die sie zu Googles … Cousin macht?), die Computertools wie AlphaFold für die Arzneimittelentwicklung einsetzt. Heutzutage nutzt jeder Computer-Tools – aber Isomorphic hatte als Erster Zugriff auf die neuesten Modelle von DeepMind und kombinierte sie mit „einigen weiteren proprietären Dingen, die mit der Arzneimittelentwicklung zu tun haben“, wie Hassabis bemerkte. Das Unternehmen unterhält bereits Partnerschaften mit Eli Lilly und Novartis.
Allerdings ist AlphaFold nicht das A und O der Biologie – nur ein sehr nützliches Werkzeug, da sind sich unzählige Forscher einig. Und es ermöglicht ihnen, das zu tun, was Max Jaderberg von Isomorphic „rationales Arzneimitteldesign“ nannte.
„Wenn wir Tag für Tag darüber nachdenken, welche Auswirkungen dies auf die Isomorphic-Labore hat: Es ermöglicht unseren Wissenschaftlern, unseren Arzneimittelentwicklern, Hypothesen auf atomarer Ebene zu erstellen und zu testen und dann innerhalb von Sekunden hochpräzise Strukturvorhersagen zu erstellen … um zu helfen.“ „Die Wissenschaftler überlegen, welche Wechselwirkungen stattfinden müssen und wie diese Designs vorangetrieben werden können, um ein gutes Medikament zu entwickeln“, sagte er. „Verglichen wird dies mit den Monaten oder sogar Jahren, die es dauern könnte, dies experimentell durchzuführen.“
Während viele die Errungenschaft und die breite Verfügbarkeit eines kostenlosen, gehosteten Tools wie AlphaFold Server feiern, weisen andere möglicherweise zu Recht darauf hin, dass dies kein wirklicher Gewinn für Open Science ist.
Wie bei vielen proprietären KI-Modellen werden der Trainingsprozess von AlphaFold und andere für die Replikation entscheidende Informationen – ein grundlegender Teil der wissenschaftlichen Methode, wie Sie sich erinnern werden – weitgehend und zunehmend zurückgehalten. Das in Nature veröffentlichte Papier geht zwar ausführlich auf die Methoden seiner Entstehung ein, es fehlen jedoch viele wichtige Details und Daten, was bedeutet, dass Wissenschaftler, die das leistungsstärkste molekularbiologische Werkzeug der Welt nutzen wollen, dies im Rahmen von „Nature“ tun müssen wachsames Auge von Alphabet, Google und DeepMind (wer weiß, wer tatsächlich die Zügel in der Hand hat).
Befürworter der offenen Wissenschaft sagen seit Jahren, dass diese Fortschritte zwar bemerkenswert sind, es aber auf lange Sicht immer besser ist, solche Dinge offen zu teilen. Auf diese Weise schreitet die Wissenschaft schließlich voran und auf diese Weise haben sich auch einige der wichtigsten Softwareprogramme der Welt entwickelt.
AlphaFold Server für alle akademischen oder nichtkommerziellen Anwendungen kostenlos zur Verfügung zu stellen, ist in vielerlei Hinsicht eine sehr großzügige Tat. Aber die Großzügigkeit von Google ist selten an Bedingungen geknüpft. Zweifellos werden viele Forscher diese Flitterwochen trotzdem nutzen, um das Modell so weit wie möglich zu nutzen, bevor die anderen Schuhe fallen.