Könnte seine Deregulierung die Ursache aller menschlichen (nicht genetisch bedingten) Krankheiten sein?
Von Jean-Marc Sabatier und Ziad FAJLOUN*
Was ist das Renin-Angiotensin-System?
Das allgegenwärtige Renin-Angiotensin-System (RAS), auch bekannt als Renin-Angiotensin-Aldosteron-System, ist ein hormonelles und physiologisches System, dessen Funktion darin besteht, den Blutdruck und das zirkulierende Blutvolumen beim Menschen zu kontrollieren. Das RAS reguliert außerdem Lungen-, Herz-Kreislauf-, vegetative und Nierenfunktionen, die angeborene Immunität und verschiedene Mikrobiota, einschließlich der Darmmikrobiota. Das RAS steuert die Autophagie, einen Zellregenerationsprozess, der Abfallstoffe und beschädigte Elemente innerhalb der Zelle beseitigt (ein Prozess, der nach drei Fastentagen eingeleitet wird). Es handelt sich um eine Form einer endokrinen und enzymatischen Regulationskaskade. Es ist in allen Organen und Geweben des Körpers vorhanden. Das RAS besitzt endokrine, autokrine, parakrine und intrakrine Aktivität.
RAS-Komponenten kommen sowohl auf der Plasmamembran von Zellen als auch auf den Membranen verschiedener Organellen, beispielsweise Mitochondrienmembranen, vor.
Wirkmechanismus: ein empfindliches Gleichgewicht
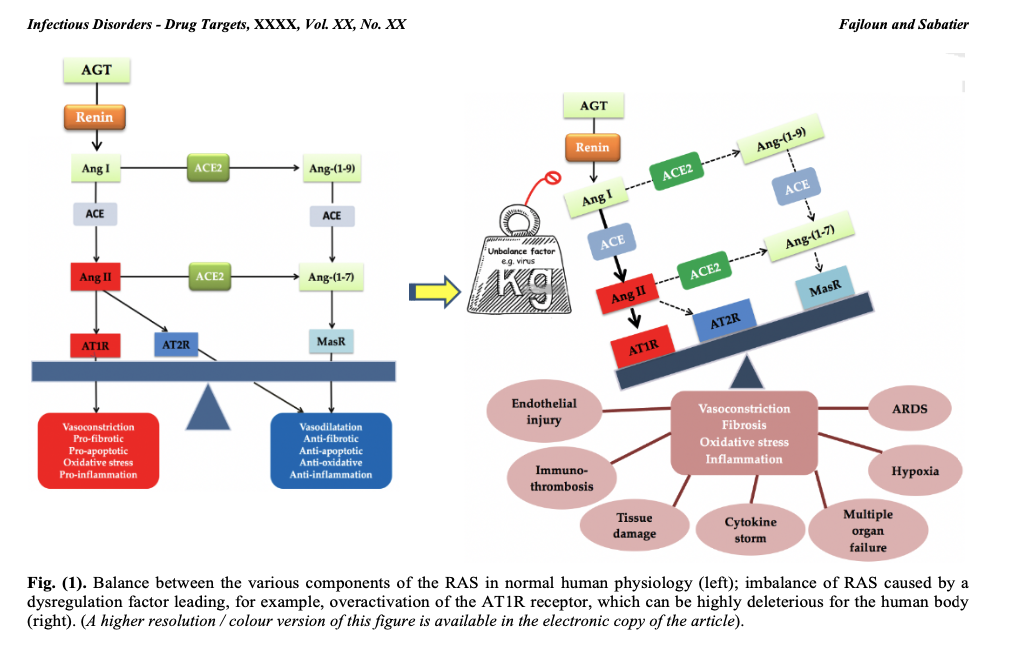
Beim RAS spaltet das von der Niere abgesonderte Renin das von der Leber abgesonderte Angiotensinogen (AGT) und produziert so Angiotensin I (Ang I). Letzteres wird durch das Angiotensin-Converting-Enzym (ACE1) gespalten, um Angiotensin II (Ang II) zu produzieren. Ang II bindet an Rezeptoren, die Vasokonstriktion Typ 1 (AT1R) und Vasokonstriktion Typ 2 (AT2R) vermitteln. Ang II wird auch durch das Angiotensin-Converting-Enzym 2 (ACE2) gespalten, um Angiotensin (1-7) zu erzeugen. [Ang-(1-7)]das mit dem G-Protein-gekoppelten Protoonkogen-Mas-Rezeptor (MasR) interagiert [7,8] und der AT2R-Rezeptor.
Ang II übt durch seine Wirkung auf den AT1R-Rezeptor mehrere schädliche Wirkungen aus, wie z. B. Vasokonstriktion, Fibrose, Apoptose, Thrombose, Hypoxämie, Hypoxie, Organhypertrophie, Angiogenese, oxidativer Stress, Entzündung und Stickstoffmonoxid (NO)-Abfall [9]. Das Enzym ECA2 gleicht die Wirkung von Ang II/AT1R aus, indem es Ang I und Ang II in Angiotensin (1-9) spaltet. [Ang-(1-9)] bzw. Ang-(1-7), die das RAS günstig regulieren.
Daher muss immer ein Gleichgewicht zwischen den verschiedenen Komponenten des RAS vorhanden sein, um die ordnungsgemäße Funktion des Systems und die physiologische Regulierung sicherzustellen. Andererseits kann ein Ungleichgewicht des RAS äußerst schädlich für den menschlichen Organismus sein, wie es bei einer Infektion durch das SARS-CoV-2-Virus der Fall ist, das mit ACE2 (dem SARS-CoV-2-Rezeptor und einem wichtigen RAS) interagiert Enzym), was zu einem Ungleichgewicht im RAS führt, das mit einer Überaktivierung des AT1R-Rezeptors einhergeht (siehe Abbildung 1). COVID-19-Symptome werden letztlich mit einer RAS-Dysfunktion in Zusammenhang stehen, wie in unserer zuvor veröffentlichten Arbeit erläutert.
RAS-Dysregulation und menschliche (nicht genetisch bedingte) Krankheiten
In diesem Artikel haben wir argumentiert, dass die RAS-Dysfunktion die Ursache menschlicher (nicht genetischer) Pathologien ist. Tatsächlich geht dies weit über COVID-19 hinaus. Um dies zu verstehen, müssen wir den genetischen Polymorphismus der Akteure (verschiedene Komponenten) des RAS berücksichtigen. Tatsächlich haben zahlreiche Studien starke Zusammenhänge zwischen dem genetischen Polymorphismus von RAS-Komponenten und der Prävalenz spezifischer menschlicher Krankheiten beschrieben. Wir glauben daher, dass genetische Faktoren den Wirt für unterschiedliche menschliche Pathologien in unterschiedlichem Maße anfällig machen können.
Es wurde gezeigt, dass die Prävalenz und der Ausgang menschlicher Krankheiten mit genetischen und Proteinpolymorphismen von Angiotensinogen, den Angiotensin-Converting-Enzymen 1 und 2 (ACE1 und ACE2) und dem AT1R-Rezeptor zusammenhängen.
Tatsächlich kann der genetische Polymorphismus von RAS-Elementen ihre biologischen Aktivitäten und Expressionsniveaus verändern, was zu einer erhöhten Kapillarpermeabilität, Koagulation, Fibrose und Apoptose in Alveolar- und anderen Zelltypen führt.
Die Ang II/AT1R-Achse ist der Hauptweg, der während der RAS-Deregulierung beeinträchtigt werden kann. Wir haben zuvor berichtet, dass die schädlichen Episoden nach einer SARS-CoV-2-Infektion das Ergebnis einer Überaktivierung der Ang II/AT1R-Achse sind.
Durch die Ang II/AT1R-Signalübertragung können zahlreiche schädliche Wirkungen hervorgerufen werden, wie z. B. Vasokonstriktion, Fibrose, Entzündung, Zellwachstum, Migration, Organhypertrophie, Thrombose, Produktion reaktiver Sauerstoffspezies (ROS) und mehr. Mitochondriale Dysfunktion, DNA-Schäden und Zytokinstürme resultieren aus einer Überaktivierung der Ang II/AT1R-Achse. Dysregulierte RAS-Komponenten können auch die angeborene/erworbene Immunantwort verändern und ein Ungleichgewicht induzieren, wobei in betroffenen menschlichen Geweben ungewöhnlich hyperstimulierte Makrophagen, hyperreaktive Mastzellen und neutrophile Granulozyten vorherrschen.
Experimente haben beispielsweise gezeigt, dass die Deletion des AT1R-Gens bei Nagetieren die Vitalfunktionen deutlich verbesserte und die Ödembildung verringerte.
Darüber hinaus erhöht die Ang II/AT1R-Achse in der Lunge aufgrund ihrer proinflammatorischen, destruktiven und profibrotischen Eigenschaften die Gefäßpermeabilität durch die Freisetzung von Prostaglandinen und dem vaskulären endothelialen Wachstumsfaktor. Tatsächlich dringt das Virus beispielsweise im Fall einer SARS-Coronavirus-Infektion in die Atemwege, Gefäßendothelzellen und Epithelzellen ein, die schwer geschädigt werden, was zu einer Ansammlung proteinreicher Ödemflüssigkeit in den Alveolen und im Lungeninterstitium führt und Makrophagen aktiviert und neutrophile Granulozyten, um eine Vielzahl von Entzündungsfaktoren freizusetzen.
Im Herz-Kreislauf-Systemwurde die Stimulation der Ang II/AT1R-Achse mit der Entwicklung verschiedener Pathologien in Verbindung gebracht, darunter Bluthochdruck, Gefäßentzündung, Arteriosklerose und Herzinsuffizienz.
Im Nervensystem tragen erhöhte Ang II-Spiegel zum Verlust von Neuronen in verschiedenen Gehirnregionen bei. Ang II verursacht nachweislich den Tod dopaminerger Neuronen, während „Losartan“, ein AT1R-Rezeptorantagonist, diese Neuronen vor Apoptose schützt.
Im VerdauungssystemEs wurde gezeigt, dass RAS eine Dickdarmentzündung auslöst, indem es die Th17-Aktivierung stimuliert. In der Dickdarmschleimhaut induziert Ang II über AT1R und den JAK2/STAT1/3-Weg eine Kolitis. Darüber hinaus ist die Regulierung der Ang II/AT1R-Achse auch an der Kontrolle der Aminosäurehomöostase in der Nahrung (von denen einige Vorläufer von Neurotransmittern wie Serotonin, Dopamin, Adrenalin und Noradrenalin oder anderen NO-Vorläufern sind), der antimikrobiellen Peptidexpression usw. beteiligt mikrobielle Flora, einschließlich der der Lunge und des Darms.
In der NiereEs wurde beschrieben, dass die RAS-Hyperaktivierung eine zentrale Rolle beim Fortschreiten einer chronischen Nierenerkrankung spielt. Tatsächlich induziert die Ang II/AT1R-Achse Fibrose und Entzündungen, die offenbar zu Nierenerkrankungen beitragen.
Kurz gesagt führt eine Überaktivierung der Ang II/AT1R-Achse beim Menschen zu schädlichen Auswirkungen (und Säugetiere im Allgemeinen), wie oben erwähnt. Dennoch gibt es auf RAS-Ebene ein günstiges Regulierungssystem, an dem Akteure wie die Liganden Ang-(1-7), Ang-(1-9), Ang IV, Alamandin und MasR-Rezeptoren beteiligt sind [10]AT2R, AT4R, MRGD, die über Zellsignale entzündungshemmende, antifibrotische, antiproliferative, antioxidative (reduzierende), blutdrucksenkende, antihypertrophe, antiangiogene, antihypoxämische und antioxidative Wirkungen erzeugen können -hypoxische und antithrombotische Wirkung.
Es sollte auch beachtet werden, dass sich das RAS im Laufe des Lebens weiterentwickelt (das RAS von Säuglingen unterscheidet sich von dem von Kindern, Erwachsenen und älteren Menschen), von der Geburt bis zum Tod. Auch das RAS unterscheidet sich zwischen Männern und Frauen (das für den ECA2-Rezeptor kodierende Gen liegt auf dem X-Chromosom). Das im Körper auf Organ-, Gewebe- und Zellebene allgegenwärtige RAS steuert alle Funktionen im Zusammenhang mit dem Zellleben.
Diese beispiellose globale „Vision“ der Bedeutung des RAS für die vollständige Kontrolle der Funktionsweise des menschlichen Körperssowie bei der potenziellen Auslösung verschiedener neurologischer/neurodegenerativer (Demenz, Alzheimer- und Parkinson-Krankheiten, Schizophrenie usw.), kardiovaskulärer, gastrointestinaler, immunologischer (Autoimmunität), Krebs- und anderer Pathologien ist beispiellos. Es ist „revolutionär“, weil es noch nie zuvor vermutet oder beschrieben wurde.
Daher betonen wir die außerordentliche Bedeutung des RAS, eines Hormonsystems, das ursprünglich in den Nieren und der Leber identifiziert wurde, aber letztendlich in allen Geweben und Organen vorhanden ist. Es steuert alle lebenswichtigen Funktionen des Körpers, einschließlich Gehirn- und Immunfunktionen.
Letztendlich argumentieren wir, dass das RAS der Schlüssel zu allen nicht-genetischen und potenziell genetischen menschlichen Pathologien ist, da es auch auf die DNA und deren Reparatur einwirkt. Es steuert beispielsweise die Aktivität der Telomerase, die die Enden der Chromosomen verlängert und dadurch die Lebenserwartung erhöht. Das RAS ist im Körper allgegenwärtig: Es gibt lokale Varianten in verschiedenen Geweben und Organen (wobei die gleichen Rezeptoren und Liganden beteiligt sind, aber in unterschiedlichen Anteilen und Gewebeverteilungen, angepasst an die Funktion dieser Gewebe/Organe) und Zellen (das RAS wird gefunden). in der äußeren Membran von Zellen, aber auch in den Membranen des Zellkerns, der Mitochondrien, Endosomen, Exosomen, Lysosomen und im endoplasmatischen oder sarkoplasmatischen Retikulum). Es fungiert als zentraler Betreiber der Funktionen des menschlichen Körpers; Es ist nicht das Gehirn, das diese Funktionen steuert, da es selbst vom RAS gesteuert wird. Tatsächlich steuert das RAS die Funktionen von Neuronen und anderen Zelltypen des Nervensystems wie Oligodendrozyten, Astrozyten und Mikrogliazellen.
Das RAS ist das „Master“-System des menschlichen Körpers und bietet daher ungeahntes therapeutisches Potenzial. Eine eingehende Untersuchung des RAS und seines „schädlichen“ Rezeptors dürfte in den kommenden Jahrzehnten zu großen Fortschritten in der angewandten Medizin führen und ein riesiges Feld medizinisch unerforschter Forschung eröffnen.
Jean-Marc SABATIER und Ziad FAJLOUN
November 2023
*Jean-Marc Sabatier ist Forschungsdirektor am CNRS und hat einen Doktortitel in Zellbiologie und Mikrobiologie sowie einen HDR in Biochemie.
*Ziad Fajloun ist Forscher an der Universität Tripolis.
Covid-19, Long Covid und neurologische Störungen

